Phản ứng Mantozo tráng bạc là một trong những phản ứng hóa học quan trọng và phổ biến trong cả nghiên cứu lẫn ứng dụng thực tiễn. Phản ứng này đặc biệt quan trọng trong việc tạo ra lớp phủ bạc trên bề mặt của các vật liệu, ứng dụng rộng rãi trong sản xuất gương, phân tích hóa học và nhiều lĩnh vực khác. Trong bài viết dưới đây hocvn sẽ đi sâu vào khái niệm, cơ chế phản ứng, điều kiện thực hiện, cũng như các ứng dụng và lưu ý an toàn khi tiến hành Phản ứng Mantozo tráng bạc.
1. Khái niệm về phản ứng Mantozo tráng bạc
1.1. Định nghĩa phản ứng tráng bạc
Phản ứng tráng bạc là một phản ứng oxy hóa khử, trong đó ion bạc (Ag⁺) trong dung dịch bạc nitrat (AgNO₃) được khử bởi một hợp chất có tính khử mạnh để tạo thành bạc kim loại (Ag). Phản ứng này thường được sử dụng để tạo ra lớp phủ bạc sáng bóng trên bề mặt vật liệu, phổ biến nhất là trên kính.
Công thức: 3C12H22O11 + 40AgNO3 + 14NH3 → 40Ag + 36CO2 + 27NH4NO3

1.2. Vai trò của Mantozo trong phản ứng
Mantozo là một loại đường đơn (monosaccharide) có khả năng khử mạnh, giúp ion Ag⁺ trong dung dịch bạc nitrat bị khử và tạo thành bạc kim loại. Khi phản ứng xảy ra, Mantozo bị oxy hóa thành axit gluconic, trong khi ion bạc bị khử thành bạc nguyên chất.
1.3. Ứng dụng của phản ứng tráng bạc
Phản ứng tráng bạc có nhiều ứng dụng trong công nghiệp, đặc biệt là trong việc sản xuất gương, đồ trang sức mạ bạc, và các ứng dụng trong phân tích hóa học. Ngoài ra, phản ứng này còn được sử dụng trong giáo dục để minh họa các quá trình oxy hóa khử.
2. Cơ chế của phản ứng tráng bạc
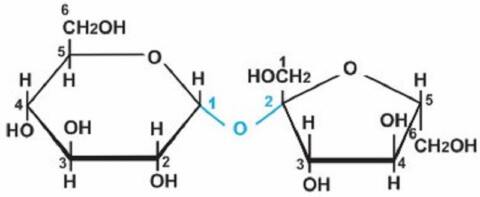
2.1. Cấu trúc hóa học của Mantozo
Mantozo là một hợp chất thuộc nhóm đường đơn (monosaccharide), có công thức hóa học là C₆H₁₂O₆. Với nhiều nhóm chức hydroxyl (-OH), Mantozo có khả năng khử ion bạc trong dung dịch bạc nitrat.
2.2. Quá trình oxy hóa khử trong phản ứng
Phản ứng tráng bạc là một quá trình oxy hóa khử, trong đó Mantozo bị oxy hóa và ion bạc (Ag⁺) bị khử. Mantozo cho đi electron, biến thành axit gluconic, trong khi ion Ag⁺ nhận electron và chuyển thành bạc kim loại, tạo thành lớp bạc sáng bóng.
2.3. Sự tạo thành lớp bạc kim loại
Lớp bạc kim loại được hình thành trên bề mặt vật liệu nhờ quá trình khử ion bạc. Bạc kim loại kết tủa dần trên bề mặt, tạo thành một lớp phủ đồng nhất và có độ sáng bóng đặc trưng.
3. Điều kiện thực hiện phản ứng Mantozo tráng bạc
3.1. Dung dịch bạc nitrat (AgNO₃)
Dung dịch bạc nitrat là nguồn cung cấp ion bạc cho phản ứng. Ion Ag⁺ từ dung dịch này sẽ bị khử để tạo thành bạc kim loại khi gặp chất khử như Mantozo.
3.2. Vai trò của ammoniac (NH₃)
Ammoniac (NH₃) có vai trò tạo phức với ion bạc, tạo ra phức bạc amoni (Ag(NH₃)₂⁺), giúp ion bạc trở nên dễ dàng tham gia vào quá trình khử hơn. Nhờ phức này, phản ứng tráng bạc có thể diễn ra trong môi trường kiềm nhẹ và dễ dàng kiểm soát.
3.3. Điều kiện nhiệt độ và pH
Phản ứng tráng bạc thường diễn ra ở nhiệt độ phòng, nhưng môi trường cần duy trì ở pH kiềm nhẹ để đảm bảo quá trình tạo phức giữa NH₃ và Ag⁺ diễn ra thuận lợi. Điều kiện kiềm giúp kiểm soát tốc độ phản ứng và tạo lớp bạc đồng đều hơn.
4. Các yếu tố ảnh hưởng đến phản ứng
4.1. Nồng độ dung dịch AgNO₃
Nồng độ dung dịch AgNO₃ quyết định lượng ion bạc có trong phản ứng. Nồng độ quá thấp có thể dẫn đến việc lớp bạc không đủ dày, trong khi nồng độ quá cao có thể làm phản ứng diễn ra quá nhanh, gây khó kiểm soát.
4.2. Nồng độ và tính chất của Mantozo
Nồng độ Mantozo ảnh hưởng trực tiếp đến tốc độ phản ứng. Một lượng Mantozo đủ để khử toàn bộ ion bạc trong dung dịch là cần thiết để đảm bảo quá trình tráng bạc diễn ra hoàn chỉnh.
4.3. Ảnh hưởng của pH môi trường
pH của môi trường phản ứng cần được kiểm soát ở mức kiềm nhẹ, để tạo điều kiện tốt nhất cho việc tạo phức bạc amoni và sự khử ion bạc. Nếu môi trường quá axit hoặc quá kiềm, phản ứng có thể bị cản trở.
4.4. Tốc độ phản ứng và điều kiện tối ưu
Tốc độ phản ứng phụ thuộc vào nhiều yếu tố, bao gồm nồng độ AgNO₃, Mantozo, và pH. Điều kiện tối ưu giúp đảm bảo phản ứng diễn ra đồng đều, lớp bạc tạo ra mịn và sáng bóng.
5. Ứng dụng thực tế của phản ứng tráng bạc
5.1. Ứng dụng trong công nghiệp sản xuất gương
Một trong những ứng dụng phổ biến nhất của phản ứng tráng bạc là trong sản xuất gương. Lớp bạc tạo ra từ phản ứng này được phủ lên mặt sau của tấm kính để tạo ra bề mặt phản chiếu hoàn hảo.
5.2. Ứng dụng trong phân tích hóa học
Phản ứng tráng bạc cũng được sử dụng trong các thí nghiệm phân tích để kiểm tra tính khử của các hợp chất hữu cơ, như aldehyde, trong phản ứng tráng gương.
5.3. Phản ứng Mantozo tráng bạc trong công nghệ mạ kim loại
Ngoài sản xuất gương, phản ứng tráng bạc còn được ứng dụng trong công nghệ mạ kim loại, giúp tạo lớp bạc mỏng trên bề mặt kim loại, tăng độ bền và giá trị thẩm mỹ cho sản phẩm.
5.4. Các ứng dụng khác trong nghiên cứu và giáo dục
Phản ứng tráng bạc thường được sử dụng trong các bài giảng hóa học để minh họa cho các khái niệm về phản ứng oxy hóa khử và sự kết tủa của kim loại.
6. Lưu ý an toàn khi thực hiện phản ứng
6.1. Biện pháp bảo hộ khi làm việc với bạc nitrat và NH₃
Bạc nitrat và NH₃ là các hóa chất có tính ăn mòn cao, do đó, khi tiến hành phản ứng, cần đeo găng tay, kính bảo hộ và làm việc trong môi trường thoáng khí để tránh hít phải hơi NH₃ độc hại.
6.2. Xử lý chất thải chứa bạc và hóa chất liên quan
Chất thải chứa bạc và các hóa chất còn sót lại sau phản ứng cần được xử lý cẩn thận theo quy định về an toàn hóa chất, tránh gây ô nhiễm môi trường.
6.3. Phòng ngừa và xử lý sự cố trong quá trình thực hiện phản ứng
Trong trường hợp tiếp xúc với bạc nitrat hoặc NH₃, cần rửa sạch ngay bằng nước và tìm kiếm sự hỗ trợ y tế nếu cần. Luôn đảm bảo có các biện pháp sơ cứu cần thiết khi thực hiện thí nghiệm.
Kết luận
Phản ứng Mantozo tráng bạc là một quá trình quan trọng trong cả nghiên cứu và ứng dụng thực tế. Từ việc tạo ra lớp bạc trong sản xuất gương đến mạ kim loại, phản ứng này mang lại nhiều giá trị và tiện ích. Tuy nhiên, để phản ứng diễn ra hiệu quả, cần đảm bảo điều kiện thực hiện và các yếu tố liên quan được kiểm soát chặt chẽ. Bên cạnh đó, tuân thủ các biện pháp an toàn là rất cần thiết để tránh nguy cơ gây hại từ các hóa chất. Hoc vn chúc các bạn học tập thật tốt nhé!
Xem thêm:
[GIẢI ĐÁP] Phản Ứng Lòng Trắng Trứng CuOH2
[GIẢI ĐÁP] Liên Kết Photphodieste Là Liên Kết Giữa Các Nguyên Tố Nào?