Giới thiệu tổng quan về phản ứng
Trong thế giới hóa học đầy màu sắc, có một phản ứng không chỉ mang tính học thuật mà còn cực kỳ đẹp mắt và ấn tượng: Phương Trình Glucozo AgNO3 NH3, hay còn được gọi là phản ứng tráng bạc. Đây là một phản ứng kinh điển trong hóa học hữu cơ, được dùng để nhận biết các hợp chất chứa nhóm chức aldehyde, như glucozo.
Khi tiến hành phản ứng, một điều kỳ diệu xảy ra: lớp bạc kim loại lấp lánh sẽ bám đều trên thành ống nghiệm, tạo ra hiệu ứng giống như một chiếc gương thật sự. Chính vì vậy, phản ứng này được gọi là phản ứng tráng gương bạc.
Vậy phản ứng này diễn ra như thế nào? Tại sao glucozo lại phản ứng với bạc nitrat trong dung dịch amoniac? Và tại sao hiện tượng này lại quan trọng đến thế trong học tập và đời sống?
Bài viết này sẽ dẫn bạn đi qua hành trình hóa học kỳ thú đó, từng bước khám phá bản chất, cơ chế, ứng dụng và những điều không ngờ tới xung quanh Phương Trình Glucozo AgNO3 NH3.
Cấu trúc và tính chất của glucozo
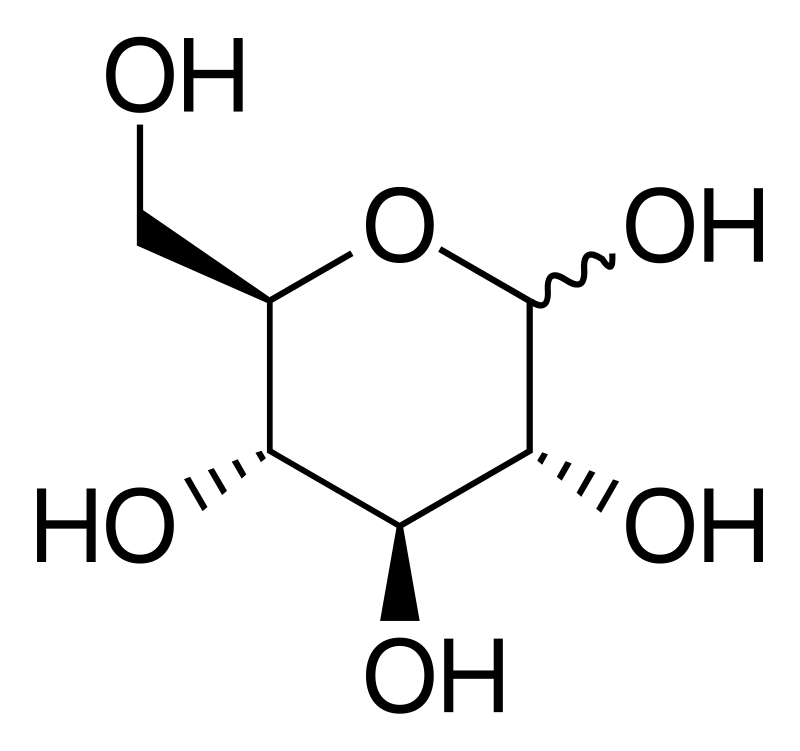
Glucozo, còn được viết là glucose trong tiếng Anh, là một loại monosaccharide – tức là đường đơn, có công thức phân tử C₆H₁₂O₆. Glucozo là một hợp chất cực kỳ quan trọng trong sinh học, là nguồn năng lượng chủ yếu cho tế bào, nhưng đồng thời nó cũng là một chất có khả năng tham gia nhiều phản ứng hóa học thú vị.
Cấu trúc phân tử của glucozo
Ở trạng thái dung dịch, glucozo có thể tồn tại ở hai dạng:
- Dạng mạch hở, với nhóm chức aldehyde (–CHO) nằm ở đầu chuỗi
- Dạng vòng, phổ biến hơn trong dung dịch nước do tính bền vững cao
Chính nhóm aldehyde là nguyên nhân khiến glucozo có tính khử – một đặc điểm then chốt để glucozo tham gia vào phản ứng với bạc nitrat trong môi trường kiềm.
Đặc điểm vật lý và hóa học
- Tan tốt trong nước
- Vị ngọt dịu
- Bị oxi hóa dễ dàng bởi các chất oxi hóa nhẹ như Ag⁺
Khi glucozo phản ứng với dung dịch AgNO₃/NH₃, nhóm aldehyde sẽ bị oxi hóa thành nhóm axit cacboxylic (–COOH), còn ion bạc (Ag⁺) sẽ bị khử thành bạc kim loại (Ag⁰).
Glucozo là một đường khử
Khái niệm “đường khử” là một thuật ngữ quan trọng trong hóa học hữu cơ. Đường khử là những loại đường có khả năng cho electron để khử các ion kim loại. Glucozo là một ví dụ điển hình. Nhờ nhóm –CHO, glucozo có thể khử ion bạc (Ag⁺) thành bạc kim loại, và hiện tượng đó chính là trọng tâm của Phương Trình Glucozo AgNO3 NH3.
Vai trò trong sinh học và công nghiệp
Trong cơ thể con người, glucozo là nhiên liệu cho não và các hoạt động sống. Trong công nghiệp thực phẩm và y tế, glucozo được dùng để:
- Làm chất tạo ngọt tự nhiên
- Sản xuất thuốc truyền dịch
- Làm nguyên liệu trong chế biến bánh kẹo
Vai trò của nhóm aldehyde trong glucozo
Phần “linh hồn” của phản ứng tráng bạc nằm ở nhóm aldehyde –CHO trong phân tử glucozo. Đây là nhóm có khả năng oxi hóa cao, và khi có mặt chất oxi hóa như ion Ag⁺ trong môi trường kiềm (do NH₃ cung cấp), phản ứng sẽ diễn ra theo kiểu phản ứng oxi hóa–khử.
Phản ứng oxi hóa của nhóm –CHO
Khi nhóm –CHO trong glucozo bị oxi hóa, nó chuyển thành –COOH, cụ thể là axit gluconic. Trong khi đó, ion Ag⁺ nhận electron và bị khử thành Ag kim loại.
Phương trình phản ứng tổng quát như sau:
C₆H₁₂O₆ + 2[Ag(NH₃)₂]⁺ + 3OH⁻ → C₆H₁₂O₇ + 2Ag↓ + 2NH₃ + 2H₂O
Lưu ý:
- [Ag(NH₃)₂]⁺ là phức ion bạc tạo bởi bạc nitrat và amoniac
- Phản ứng cần môi trường kiềm nhẹ (do NH₃ cung cấp)
- Kết tủa bạc xuất hiện dưới dạng lớp gương sáng trên thành ống nghiệm
So sánh với các loại đường khác
Không phải loại đường nào cũng có khả năng tham gia phản ứng này. Ví dụ:
- Fructozo cũng là đường khử nhưng không có nhóm –CHO ở dạng mạch hở nên phản ứng xảy ra chậm hơn
- Sucrozo (đường mía) không phải đường khử, nên không phản ứng với AgNO₃/NH₃
Chính vì thế, phản ứng này được sử dụng trong phòng thí nghiệm để phân biệt các loại đường.
Giới thiệu về bạc nitrat (AgNO₃)
Bạc nitrat – hay còn gọi là AgNO₃ – là một hợp chất vô cơ rất quen thuộc trong hóa học. Nó tồn tại ở dạng tinh thể màu trắng, tan tốt trong nước và có khả năng phản ứng nhanh với các chất khử, đặc biệt là các hợp chất chứa nhóm chức aldehyde như glucozo. Đây chính là một trong những chất đóng vai trò trung tâm trong Phương Trình Glucozo AgNO3 NH3.
Tính chất hóa học và vật lý nổi bật
- Công thức phân tử: AgNO₃
- Khối lượng mol: khoảng 169.87 g/mol
- Trạng thái: rắn, màu trắng
- Đặc điểm: tan hoàn toàn trong nước, nhạy cảm với ánh sáng (có thể chuyển sang màu xám khi để ngoài sáng quá lâu)
Bạc nitrat là một muối có tính oxi hóa mạnh. Khi hòa tan trong nước, nó phân ly thành:
- Ion bạc (Ag⁺)
- Ion nitrat (NO₃⁻)
Trong môi trường có mặt amoniac (NH₃), ion Ag⁺ sẽ tạo thành phức chất [Ag(NH₃)₂]⁺, giúp bạc tồn tại lâu hơn trong dung dịch mà không kết tủa ngay.

Ứng dụng của AgNO₃ trong thực tế
- Trong hóa học phân tích: dùng để xác định sự có mặt của các nhóm chức như –CHO.
- Trong y học: có tính khử khuẩn, được dùng trong một số dung dịch sát trùng.
- Trong chế tạo gương: phản ứng tráng bạc là tiền đề để sản xuất gương kính truyền thống.
- Trong giáo dục: là chất không thể thiếu trong các thí nghiệm minh họa phản ứng oxi hóa–khử.
Cần lưu ý gì khi sử dụng AgNO₃?
AgNO₃ tuy không độc mạnh nhưng vẫn cần được xử lý cẩn thận:
- Có thể gây bỏng nhẹ nếu dính vào da
- Gây đen da vì phản ứng với các chất hữu cơ
- Phải đeo găng tay, kính bảo hộ khi sử dụng
- Không nên đổ xuống cống sau khi dùng – cần xử lý đúng cách
Dung dịch amoniac (NH₃) và vai trò trong phản ứng
Amoniac (NH₃) là một hợp chất khí, khi hòa tan vào nước sẽ tạo thành dung dịch kiềm yếu – còn gọi là amoniac. Trong Phương Trình Glucozo AgNO3 NH3, NH₃ đóng vai trò cực kỳ quan trọng: nó không chỉ cung cấp môi trường kiềm, mà còn giúp ổn định ion bạc bằng cách tạo phức.
Tính chất và vai trò hóa học
- NH₃ là bazơ yếu nhưng có khả năng tạo liên kết với ion kim loại.
- Khi cho NH₃ vào dung dịch AgNO₃, sẽ xảy ra hai bước:
- Lúc đầu, bạc tạo kết tủa AgOH
- Nhưng kết tủa này tan trong dư NH₃, tạo thành phức [Ag(NH₃)₂]⁺ – chính là thuốc thử Tollens
Phức chất này có khả năng tồn tại bền trong môi trường kiềm và sẽ tham gia phản ứng với glucozo.
Cơ chế phản ứng
- Glucozo là chất khử, nên sẽ nhường electron cho Ag⁺
- Ag⁺ trong phức chất bị khử thành Ag (kim loại) → bám lên thành ống nghiệm
- Đây là hiện tượng tạo “gương bạc” nổi tiếng trong hóa học phổ thông
Tính chất an toàn của NH₃
- Mùi khai đặc trưng, có thể gây khó chịu nếu hít nhiều
- Cần làm việc trong tủ hút khí hoặc phòng thoáng
- Tránh tiếp xúc trực tiếp với mắt và da
Cách tạo thuốc thử Tollens
Thuốc thử Tollens là dung dịch chứa ion bạc trong môi trường amoniac, được sử dụng để nhận biết các hợp chất chứa nhóm chức aldehyde như glucozo. Đây là dung dịch mà bạn sẽ cần để thực hiện Phương Trình Glucozo AgNO3 NH3 thành công.
Nguyên liệu cần chuẩn bị
- Dung dịch bạc nitrat (AgNO₃) 0,1M
- Dung dịch amoniac loãng (NH₃ ~1–2%)
- Dung dịch natri hydroxide (NaOH) loãng
Các bước tiến hành
- Nhỏ vài giọt AgNO₃ vào ống nghiệm sạch.
- Thêm từ từ NaOH cho đến khi xuất hiện kết tủa nâu xám của Ag₂O.
- Nhỏ tiếp NH₃ vào kết tủa vừa tạo đến khi kết tủa tan hoàn toàn → dung dịch trở nên trong suốt.
- Dung dịch lúc này chính là thuốc thử Tollens – sẵn sàng để phản ứng với glucozo.
Lưu ý quan trọng
- Dung dịch Tollens nên được sử dụng ngay sau khi điều chế.
- Nếu để lâu, có thể tạo ra hợp chất nổ như bạc fulminat (Ag₂C₂N₂O₂), rất nguy hiểm.
- Luôn rửa sạch ống nghiệm và không để dung dịch tồn đọng sau thí nghiệm.
Phân tích chi tiết Phương Trình Glucozo AgNO3 NH3
Đây là phần trọng tâm nhất của bài viết – nơi chúng ta sẽ “mổ xẻ” phản ứng tráng bạc nổi tiếng từng bước một. Phản ứng này không chỉ là bài học kinh điển trong chương trình hóa học phổ thông, mà còn là một minh chứng sống động cho phản ứng oxi hóa – khử trong thực tế.
Phương trình tổng quát
Phản ứng giữa glucozo với thuốc thử Tollens (AgNO₃ trong NH₃) được viết như sau:
C₆H₁₂O₆ + 2[Ag(NH₃)₂]⁺ + 3OH⁻ → C₆H₁₂O₇ + 2Ag↓ + 2NH₃ + 2H₂O
Trong đó:
- C₆H₁₂O₆ là glucozo (chất khử)
- [Ag(NH₃)₂]⁺ là phức bạc trong dung dịch Tollens (chất oxi hóa)
- C₆H₁₂O₇ là axit gluconic (sản phẩm oxi hóa)
- Ag↓ là bạc kim loại tạo thành → tạo ra hiện tượng “gương bạc” đẹp mắt
Giải thích từng thành phần
- Glucozo: chất có nhóm –CHO, dễ bị oxi hóa.
- Phức bạc [Ag(NH₃)₂]⁺: được tạo ra từ bạc nitrat và amoniac, giúp bạc tan trong dung dịch kiềm và dễ phản ứng.
- OH⁻: tạo môi trường kiềm cần thiết để phản ứng xảy ra thuận lợi.
- Bạc kim loại (Ag): xuất hiện dưới dạng kết tủa sáng bóng bám lên thành ống nghiệm – điểm nhấn đặc trưng của phản ứng.
Cơ chế phản ứng đơn giản hóa
- Ion bạc Ag⁺ nhận electron từ glucozo → bị khử thành bạc kim loại
- Nhóm –CHO trong glucozo bị oxi hóa thành nhóm –COOH
- Phản ứng tạo ra bạc nguyên chất và dung dịch amoniac quay trở lại
Những điểm cần chú ý khi viết và hiểu phương trình
- Sử dụng đúng dạng phức bạc, không viết AgNO₃ đơn thuần
- Phải có mặt của ion OH⁻ để duy trì môi trường kiềm
- Sản phẩm là bạc kim loại (Ag), không phải muối bạc khác
Tại sao phản ứng lại quan trọng đến thế?
- Giúp nhận biết nhóm chức –CHO một cách chính xác
- Là phản ứng đặc trưng cho aldehyde, trong đó glucozo là một đại diện tiêu biểu
- Là cơ sở cho các thí nghiệm tráng bạc trong công nghiệp sản xuất gương thủ công
Hiện tượng tráng bạc và minh họa thực tế
Một trong những lý do khiến Phương Trình Glucozo AgNO3 NH3 được yêu thích trong giáo dục là bởi nó tạo ra hiện tượng đẹp mắt mà học sinh nào cũng phải “ồ” lên khi nhìn thấy. Đó chính là hiện tượng tráng bạc – lớp bạc sáng bóng phủ đều lên thành ống nghiệm, giống như một chiếc gương thật sự.
Mô tả hiện tượng
- Dung dịch Tollens trong suốt ban đầu
- Khi cho glucozo vào và đun nhẹ, thành ống nghiệm bắt đầu xuất hiện lớp bạc mỏng
- Sau vài phút, bạc kết tinh phủ đều thành một lớp sáng bóng như gương
- Nếu ống nghiệm được xoay nhẹ trong quá trình phản ứng, lớp bạc sẽ phủ đều và đồng nhất
Tại sao lại gọi là “gương bạc”?
- Vì lớp bạc bám vào thành ống nghiệm có độ phản xạ ánh sáng cao, giống hệt bề mặt của gương
- Đây cũng là cách người ta từng sản xuất gương thủ công trong quá khứ: tráng bạc lên mặt kính bằng phản ứng hóa học
Ứng dụng của hiện tượng
- Trong học tập: minh họa phản ứng oxi hóa – khử, nhận biết aldehyde
- Trong công nghiệp: sản xuất gương, trang trí pha lê, tạo lớp bạc bảo vệ
- Trong thủ công mỹ nghệ: tạo lớp bạc mỏng phủ lên các vật thể như vỏ chai, bóng thủy tinh
Phản ứng tráng bạc – Di sản hóa học cổ điển
Phản ứng tráng bạc không chỉ có giá trị khoa học, mà còn là một phần di sản quý báu của hóa học cổ điển. Nó được phát hiện và sử dụng từ thế kỷ 19 và vẫn còn nguyên giá trị cho đến ngày nay.
Lịch sử phát hiện
- Vào những năm 1800, nhà hóa học người Đức Bernhard Tollens đã phát triển thuốc thử Tollens để nhận biết aldehyde
- Phát minh của ông đã mở đường cho kỹ thuật nhận biết hợp chất hữu cơ
- Cho đến nay, thuốc thử Tollens vẫn được dùng phổ biến trong chương trình học phổ thông và đại học
Tại sao phản ứng này được ưa chuộng lâu dài?
- Phản ứng rõ ràng, dễ quan sát
- Có giá trị minh họa trực quan
- Dễ thực hiện với dụng cụ cơ bản
Ảnh hưởng trong giáo dục
- Học sinh dễ nhớ nhờ hiện tượng “gương bạc” nổi bật
- Giúp nâng cao kỹ năng thí nghiệm, phân tích và quan sát
- Là bước đệm để hiểu sâu hơn về hóa hữu cơ và phản ứng oxi hóa – khử
So sánh phản ứng với các loại đường khác
Một trong những điều quan trọng khi học về phản ứng tráng bạc là biết loại đường nào có thể phản ứng và loại nào thì không. Không phải tất cả các loại đường đều có khả năng tạo ra “gương bạc” như glucozo. Việc này phụ thuộc chủ yếu vào sự hiện diện của nhóm chức aldehyde (–CHO) trong phân tử.
Glucozo và phản ứng tráng bạc
- Có nhóm –CHO tự do trong cấu trúc mạch hở
- Phản ứng nhanh và rõ ràng với thuốc thử Tollens
- Tạo lớp bạc sáng bóng sau vài phút
Fructozo (C₆H₁₂O₆) – đường trái cây
- Là ketose (có nhóm chức ketone –CO–), không phải aldehyde
- Tuy nhiên, trong môi trường kiềm, fructozo có thể chuyển hóa thành glucozo thông qua quá trình đồng phân hóa → sau đó phản ứng như glucozo
- Phản ứng diễn ra nhưng chậm hơn và ít rõ ràng hơn
Sucrozo (đường mía)
- Là disaccharide (gồm glucozo + fructozo)
- Không có nhóm chức –CHO tự do
- Không phản ứng với thuốc thử Tollens → không tạo gương bạc
Maltose và lactose
- Là disaccharide có liên kết glycosid dễ bị thủy phân
- Trong điều kiện kiềm, có thể giải phóng glucozo → có thể tham gia phản ứng tráng bạc
- Tuy nhiên, phản ứng yếu hơn so với glucozo nguyên chất
Tóm tắt bằng bảng so sánh:
| Loại đường | Nhóm chức | Phản ứng tráng bạc | Ghi chú bổ sung |
|---|---|---|---|
| Glucozo | Aldehyde | Có | Phản ứng mạnh, tạo gương rõ |
| Fructozo | Ketone | Có (gián tiếp) | Cần môi trường kiềm để chuyển hóa |
| Sucrozo | Không có | Không | Không có nhóm –CHO tự do |
| Maltose/Lactose | Aldehyde (ẩn) | Có (yếu) | Phản ứng yếu, cần thủy phân một phần |
Ý nghĩa giáo dục và học thuật của phản ứng
Phản ứng Phương Trình Glucozo AgNO3 NH3 không chỉ là một bài tập hóa học đơn thuần, mà còn là một công cụ giảng dạy cực kỳ hiệu quả trong giáo dục phổ thông và đại học.
Giá trị giảng dạy trực quan
- Dễ quan sát: lớp gương bạc tạo hiệu ứng thị giác ấn tượng
- Dễ ghi nhớ: học sinh sẽ nhớ lâu nhờ hình ảnh sinh động
- Dễ thực hiện: chỉ cần vài hóa chất cơ bản là có thể thực hành
Gắn kết giữa lý thuyết và thực hành
- Lý thuyết về oxi hóa – khử trở nên dễ hiểu hơn khi chứng kiến thực tế
- Học sinh học cách viết phương trình ion, cân bằng điện tích
- Hiểu rõ vai trò từng thành phần trong phản ứng (chất khử, chất oxi hóa, xúc tác)
Phát triển kỹ năng thí nghiệm
- Cách sử dụng ống nghiệm, pipet, đèn cồn
- Kỹ năng pha chế dung dịch đúng quy trình
- Cách quan sát và ghi lại hiện tượng một cách khoa học
Mở rộng tư duy hóa học
- Liên hệ với các phản ứng khác: Fehling, Benedict
- Tìm hiểu về cấu trúc phân tử, liên kết phức
- Giải thích tại sao có sự chọn lọc nhóm chức
Phản ứng trong công nghiệp và đời sống
Dù phản ứng tráng bạc thường xuất hiện trong sách giáo khoa, nhưng ít ai biết rằng nó từng là nền tảng của cả một ngành công nghiệp – sản xuất gương truyền thống.
Ứng dụng trong sản xuất gương
- Trước khi có kỹ thuật tráng nhôm hiện đại, bạc là vật liệu chính dùng để tráng lên kính
- Phản ứng glucozo – AgNO₃ – NH₃ là phương pháp tạo lớp phủ bạc cực mịn trên mặt kính
- Tuy mất dần vai trò trong công nghiệp hiện đại, nhưng vẫn được dùng trong sản xuất đồ thủ công mỹ nghệ cao cấp
Kiểm nghiệm hóa chất trong thực phẩm
- Kiểm tra sự hiện diện của đường khử trong thực phẩm
- Nhận biết glucozo trong các mẫu mẫu kiểm nghiệm
Trong nghiên cứu hóa học
- Dùng để phân biệt các hợp chất hữu cơ có chứa aldehyde
- Là phản ứng mẫu để nghiên cứu tính chất chất khử
Sai lầm phổ biến khi thực hiện phản ứng
Ngay cả những bạn học sinh giỏi hóa cũng có thể mắc một số lỗi khi làm phản ứng này. Hãy cùng điểm qua để tránh sai lầm:
Không tạo đủ môi trường kiềm
- Không thêm đủ NH₃ → bạc không tạo phức → không có phản ứng
Dùng glucozo quá loãng hoặc quá đặc
- Nồng độ không phù hợp có thể khiến phản ứng chậm hoặc kết quả không rõ ràng
Đun quá lâu hoặc nhiệt độ quá cao
- Bạc có thể kết tủa lộn xộn, không phủ thành lớp gương
Không dùng ống nghiệm sạch
- Tạp chất trên thành ống nghiệm sẽ ngăn cản bạc bám đều → gương loang lổ
Cách khắc phục
- Sử dụng ống nghiệm sạch, khô
- Pha đúng tỉ lệ thuốc thử Tollens
- Cho glucozo vừa đủ và đun nhẹ tay
- Không để phản ứng quá lâu
Thí nghiệm tại nhà hoặc trường học – Có thể không?
Thí nghiệm phản ứng tráng bạc không chỉ mang tính lý thuyết, mà hoàn toàn có thể thực hiện được tại trường học, thậm chí là tại nhà nếu có đầy đủ dụng cụ và tuân thủ nghiêm ngặt an toàn hóa học. Đây là một hoạt động thú vị, giúp học sinh trực tiếp chứng kiến sự chuyển hóa hóa học qua hiện tượng cực kỳ bắt mắt.
Dụng cụ cần chuẩn bị
- 1 ống nghiệm sạch
- Pipet hoặc ống nhỏ giọt
- Đèn cồn hoặc bếp mini
- Kẹp gỗ, giá đỡ ống nghiệm
- Găng tay, kính bảo hộ
Hóa chất cần có
- Dung dịch bạc nitrat (AgNO₃) 0,1M
- Dung dịch natri hydroxide (NaOH) loãng
- Dung dịch amoniac (NH₃) loãng
- Dung dịch glucozo (hoặc viên C sủi không đường)
Các bước tiến hành
- Tạo thuốc thử Tollens:
- Nhỏ vài giọt AgNO₃ vào ống nghiệm
- Thêm từ từ NaOH → xuất hiện kết tủa nâu xám (Ag₂O)
- Nhỏ tiếp NH₃ cho đến khi kết tủa tan hoàn toàn → dung dịch trong suốt
- Cho glucozo vào:
- Nhỏ vài giọt dung dịch glucozo vào ống nghiệm
- Lắc nhẹ, sau đó đun cách thủy hoặc hơ nhẹ dưới lửa
- Quan sát hiện tượng:
- Sau vài phút, lớp bạc sáng bóng xuất hiện bám vào thành ống nghiệm
Lưu ý an toàn:
- Tuyệt đối không để dung dịch Tollens lâu vì có thể sinh chất nổ nhẹ
- Không hít khí amoniac
- Đổ bỏ hóa chất thí nghiệm theo đúng quy trình môi trường
Thí nghiệm này vừa đơn giản, vừa tạo cảm hứng học hóa cho học sinh và người mới bắt đầu. Và chắc chắn, không ai quên được vẻ đẹp của chiếc “gương bạc” tự tạo đầu tiên trong đời!
Câu hỏi thường gặp (FAQs)
1. Phản ứng Phương Trình Glucozo AgNO3 NH3 xảy ra ở điều kiện nào?
Phản ứng xảy ra tốt trong môi trường kiềm nhẹ, có thuốc thử Tollens (AgNO₃ + NH₃), và có thể đun nóng nhẹ để thúc đẩy phản ứng.
2. Tại sao glucozo phản ứng được còn fructozo lại yếu hơn?
Glucozo có nhóm –CHO tự do nên phản ứng mạnh. Fructozo là ketose, không có nhóm aldehyde nhưng có thể đồng phân hóa sang glucozo trong môi trường kiềm → phản ứng yếu hơn.
3. Có thể thay NH₃ bằng chất kiềm khác không?
Không thể. NH₃ không chỉ tạo môi trường kiềm mà còn giúp tạo phức bạc [Ag(NH₃)₂]⁺, là thành phần quan trọng nhất trong thuốc thử Tollens.
4. Có phải loại đường nào cũng phản ứng với Tollens không?
Không. Chỉ các đường khử như glucozo, fructozo (ở mức độ thấp) hoặc maltose mới phản ứng. Sucrozo thì không phản ứng.
5. Vì sao phải dùng ống nghiệm sạch và khô?
Bạc chỉ bám tốt trên bề mặt sạch hoàn toàn. Nếu có dầu mỡ, tạp chất, lớp bạc sẽ loang lổ, xấu và không tạo “gương”.
6. Có thể dùng phản ứng này để kiểm tra glucozo trong thực phẩm không?
Có, nhưng không chính xác tuyệt đối. Phản ứng cho biết có đường khử, không phân biệt riêng glucozo hay loại đường nào khác.
Kết luận: Tầm quan trọng và vẻ đẹp hóa học của Phương Trình Glucozo AgNO3 NH3
Phản ứng giữa glucozo, bạc nitrat và amoniac – hay chính xác hơn là Phương Trình Glucozo AgNO3 NH3 – không chỉ là một phương trình hóa học khô khan. Nó là một minh chứng sinh động cho vẻ đẹp của phản ứng oxi hóa – khử, là công cụ giảng dạy trực quan tuyệt vời, và từng là nền tảng cho kỹ thuật sản xuất gương trong lịch sử nhân loại.
Qua bài phân tích của hocvn, bạn sẽ thấy ở nhiều gốc độ. Như từ góc nhìn của người học, nó giúp rèn luyện tư duy logic, phản xạ phân tích, và trên hết là tạo sự hứng thú với môn Hóa học. Cũng như từ góc nhìn của nhà giáo dục, đây là bài học vừa dễ nhớ vừa mang tính ứng dụng cao. Còn từ góc nhìn của nhà khoa học, phản ứng này gợi nhớ đến một thời kỳ hóa học cổ điển đầy sáng tạo.
Nếu bạn chưa từng tự tay tạo ra “gương bạc” bằng phản ứng glucozo với Tollens, thì đây là lúc để thử! Hóa học không hề xa vời – nó là ánh bạc lấp lánh trong chính lòng bàn tay bạn.
Xem thêm: