Ion đơn nguyên tử là khái niệm cơ bản trong hóa học, liên quan đến các hạt mang điện tích, được hình thành từ một nguyên tử duy nhất. Trong nhiều phản ứng hóa học và quá trình sinh học, ion đơn nguyên tử đóng vai trò quan trọng. Vậy Ion Nào Sau Đây Là Ion Đơn Nguyên Tử ? là câu hỏi của nhiều bạn học viên, cũng như làm thế nào để phân biệt chúng với các loại ion khác? Hocvn sẽ cung cấp câu trả lời cho những câu hỏi trên và giúp bạn hiểu rõ hơn về tính chất của các ion đơn nguyên tử.
1. Định Nghĩa Ion Đơn Nguyên Tử
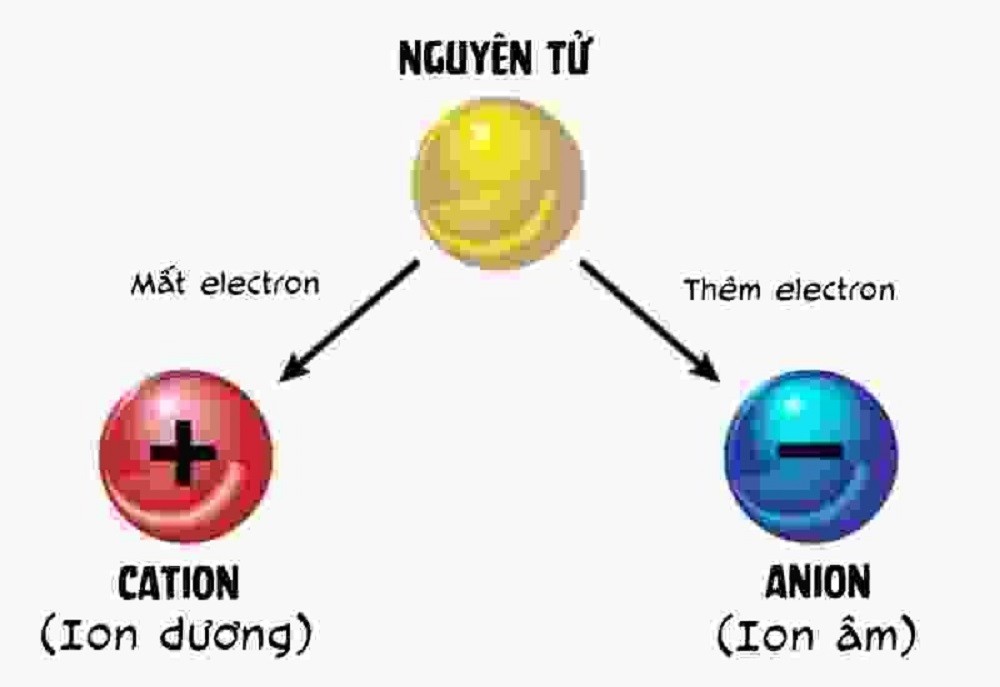
Ion đơn nguyên tử là loại ion được hình thành từ một nguyên tử duy nhất khi nguyên tử đó mất hoặc nhận thêm electron, từ đó mang điện tích dương hoặc âm. Điều này xảy ra khi nguyên tử cố gắng đạt được trạng thái ổn định tương tự như các nguyên tố khí hiếm trong bảng tuần hoàn.
Ví dụ:
- Na⁺: Ion natri được tạo ra khi nguyên tử natri (Na) mất đi 1 electron, tạo thành ion mang điện tích dương.
- Cl⁻: Ion clo được tạo ra khi nguyên tử clo (Cl) nhận thêm 1 electron, tạo thành ion mang điện tích âm.
2. Phân Loại Ion Đơn Nguyên Tử
Ion đơn nguyên tử có thể được chia thành hai loại chính:
2.1. Ion Dương Đơn Nguyên Tử (Cation)
Cation là những ion mang điện tích dương, được hình thành khi một nguyên tử mất đi một hoặc nhiều electron. Các nguyên tử kim loại như natri (Na), kali (K), và canxi (Ca) thường tạo ra các ion dương.
Ví dụ:
- Na⁺: Natri mất 1 electron.
- Ca²⁺: Canxi mất 2 electron.
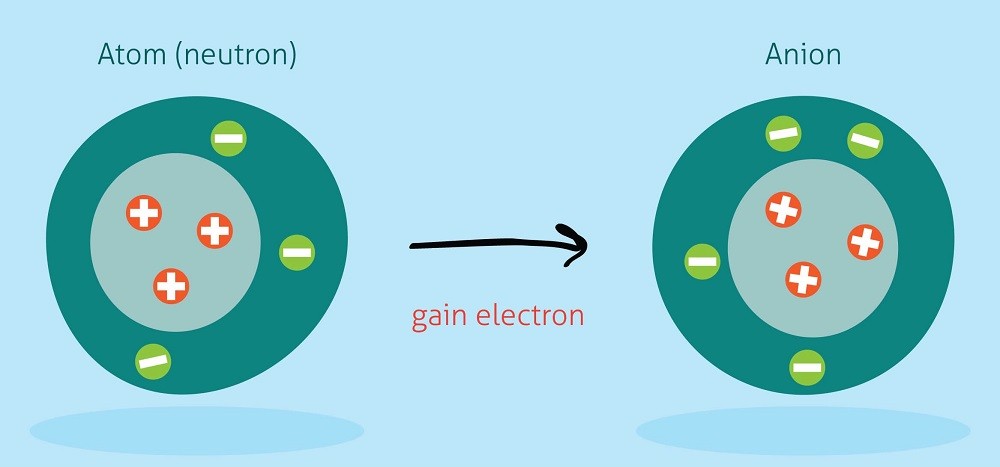
2.2. Ion Âm Đơn Nguyên Tử (Anion)
Anion là những ion mang điện tích âm, hình thành khi một nguyên tử nhận thêm electron. Các nguyên tử phi kim như clo (Cl), flo (F), và oxy (O) thường tạo ra các ion âm.
Ví dụ:
- Cl⁻: Clo nhận 1 electron.
- O²⁻: Oxy nhận 2 electron.
3. So Sánh Ion Đơn Nguyên Tử Và Ion Đa Nguyên Tử
3.1. Ion Đa Nguyên Tử Là Gì?
Ion đa nguyên tử là các ion được hình thành từ hai hoặc nhiều nguyên tử liên kết với nhau và mang điện tích. Điển hình là các nhóm ion như NO₃⁻ (nitrate), SO₄²⁻ (sulfate), và NH₄⁺ (amoni). Những ion này thường tham gia vào các phản ứng hóa học phức tạp.
3.2. Sự Khác Biệt Giữa Ion Đơn Nguyên Tử Và Ion Đa Nguyên Tử
- Ion đơn nguyên tử: Chỉ gồm một nguyên tử duy nhất (ví dụ: Na⁺, Cl⁻).
- Ion đa nguyên tử: Gồm nhiều nguyên tử liên kết với nhau (ví dụ: SO₄²⁻, NO₃⁻).
Việc phân biệt giữa ion đơn nguyên tử và ion đa nguyên tử rất quan trọng trong các bài tập hóa học, giúp xác định đúng tính chất và vai trò của các ion trong phản ứng.
4. Cách Xác Định Ion Đơn Nguyên Tử
4.1. Phân Biệt Dựa Trên Ký Hiệu Hóa Học
Để xác định ion đơn nguyên tử, bạn có thể dựa vào ký hiệu hóa học. Nếu ion chỉ bao gồm một nguyên tố, đó là ion đơn nguyên tử. Ví dụ:
- Na⁺ là ion đơn nguyên tử vì chỉ có một nguyên tố natri (Na).
- Cl⁻ là ion đơn nguyên tử vì chỉ có một nguyên tố clo (Cl).
Trong khi đó, SO₄²⁻ (sulfate) là ion đa nguyên tử vì bao gồm nhiều nguyên tử (lưu huỳnh và oxy).
4.2. Sử Dụng Bảng Tuần Hoàn
Các nguyên tố thuộc nhóm kim loại kiềm (như Na, K) và kim loại kiềm thổ (như Ca, Mg) thường tạo ra các cation đơn nguyên tử, trong khi các nguyên tố phi kim thuộc nhóm halogen (như Cl, F) thường tạo ra các anion đơn nguyên tử.
5. Cách Các Ion Đơn Nguyên Tử Hình Thành
Ion đơn nguyên tử hình thành từ quá trình mất hoặc nhận electron của nguyên tử. Trong quá trình này, nguyên tử mất đi hoặc nhận thêm electron để đạt được cấu hình electron ổn định hơn. Điều này giúp chúng có tính chất tương tự như các khí hiếm, vốn có cấu hình electron bền vững.
Ví dụ:
- Na⁺: Nguyên tử natri (Na) mất 1 electron, tạo thành ion dương (cation).
- Cl⁻: Nguyên tử clo (Cl) nhận thêm 1 electron, tạo thành ion âm (anion).
6. Tính Chất Của Ion Đơn Nguyên Tử
6.1. Tính Chất Hóa Học
Ion đơn nguyên tử có tính chất phản ứng mạnh trong các dung dịch và thường tham gia vào các phản ứng hóa học như kết tủa hoặc trung hòa. Ví dụ, khi Na⁺ và Cl⁻ gặp nhau trong nước, chúng sẽ tạo thành muối NaCl (natri clorua).
6.2. Vai Trò Trong Cơ Thể Sống
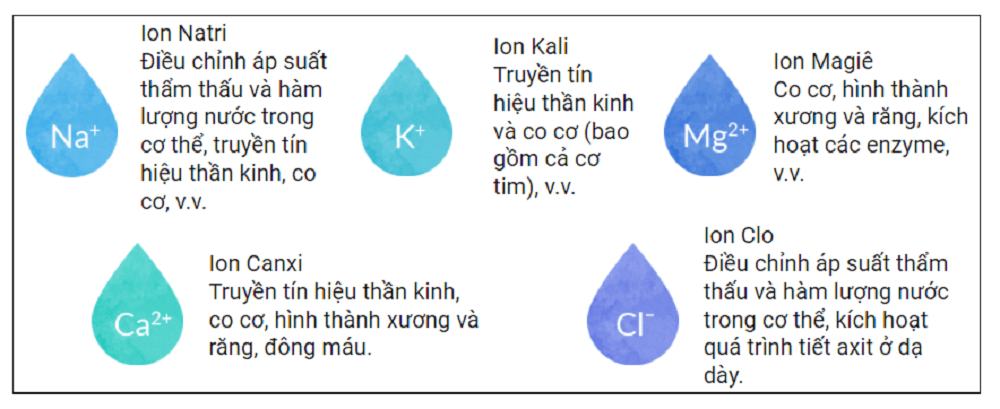
Trong cơ thể người, các ion đơn nguyên tử như Na⁺, K⁺, và Cl⁻ đóng vai trò quan trọng trong việc duy trì cân bằng điện giải, truyền dẫn tín hiệu thần kinh và điều chỉnh áp suất thẩm thấu.
7. Ứng Dụng Của Ion Đơn Nguyên Tử Trong Đời Sống Và Công Nghiệp
7.1. Ứng Dụng Trong Công Nghiệp
- Na⁺ và Cl⁻ là các ion đơn nguyên tử phổ biến trong sản xuất muối, xử lý nước và sản xuất các hóa chất công nghiệp.
- Ca²⁺ được sử dụng rộng rãi trong xây dựng, sản xuất xi măng và cải thiện đất nông nghiệp.
7.2. Ứng Dụng Trong Y Học
- K⁺ và Ca²⁺ có vai trò quan trọng trong việc duy trì chức năng của cơ bắp, hệ thần kinh và tim mạch. Chúng thường được sử dụng trong các liệu pháp điều trị các rối loạn liên quan đến điện giải.
8. Mối Liên Hệ Với Các Phản Ứng Hóa Học
Ion đơn nguyên tử tham gia vào nhiều loại phản ứng hóa học, từ phản ứng trung hòa đến phản ứng kết tủa. Ví dụ, ion H⁺ và OH⁻ kết hợp với nhau trong phản ứng trung hòa để tạo ra nước:
H⁺+OH⁻→H₂O
Trong phản ứng kết tủa, ion Ag⁺ kết hợp với ion Cl⁻ để tạo thành muối kết tủa AgCl:
Ag⁺+Cl⁻→AgCl (kết tủa)
Kết Luận
Ion đơn nguyên tử là các hạt mang điện tích được hình thành từ một nguyên tử duy nhất. Chúng đóng vai trò quan trọng trong cả các quá trình hóa học và sinh học. Với tính chất đơn giản nhưng mạnh mẽ, các ion đơn nguyên tử như Na⁺, K⁺, và Cl⁻ có ứng dụng rộng rãi trong đời sống, công nghiệp và y học. Hiểu rõ về ion đơn nguyên tử giúp chúng ta dễ dàng phân biệt chúng với các ion đa nguyên tử và áp dụng chúng vào nhiều lĩnh vực khác nhau.
Bài viết về Ion Nào Sau Đây Là Ion Đơn Nguyên Tử ? đã cung cấp cái nhìn tổng quan và chi tiết về ion đơn nguyên tử, từ khái niệm cơ bản, cách phân loại đến ứng dụng thực tế trong đời sống. Hoc vn hi vọng đã giải đáp thắc mắc cho các bạn và chúc các bạn học tập thật tốt nhé!
Xem thêm:
[GIẢI ĐÁP] Nguyên Tử Đồng Có Hai Đồng Vị Chúng Khác Nhau Về Điều Gì?
[TÌM HIỂU] Phản Ứng Hóa Học Giữa Fe2O3 CO Dư