Giới Thiệu Về Phương Trình Điện Li Al₂(SO₄)₃
Phương trình điện li là quá trình phân tách các hợp chất trong dung dịch thành các ion. Trong trường hợp của nhôm sunfat, hay Al₂(SO₄)₃, quá trình điện li xảy ra khi hợp chất này được hòa tan trong nước, dẫn đến sự phân ly thành các ion nhôm (Al³⁺) và các ion sunfat (SO₄²⁻). Hãy cùng hocvn tìm hiểu rõ “Phương Trình Điện Li Al2 SO4 3 Là Gì?”, không chỉ giúp chúng ta nắm vững nguyên tắc cơ bản của hóa học mà còn thấy được ứng dụng thực tế trong nhiều ngành công nghiệp và khoa học.
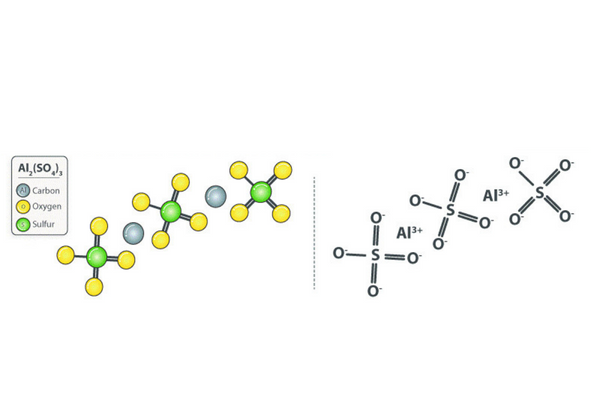
Nguyên Tắc và Cách Thức Điện Li
Quá trình điện li của Al₂(SO₄)₃ diễn ra theo nguyên tắc rằng các phân tử hợp chất ion khi hòa tan trong nước sẽ bị phân ly thành các ion tự do. Phương trình điện li của nhôm sunfat có dạng như sau:
Al2(SO4)3→2Al3++3SO2–4
Các yếu tố ảnh hưởng đến quá trình điện li bao gồm:
- Nồng độ dung dịch: Nồng độ của Al₂(SO₄)₃ trong nước ảnh hưởng đến mức độ phân li, với nồng độ cao hơn thường dẫn đến sự phân li nhiều hơn.
- Nhiệt độ: Nhiệt độ càng cao, quá trình điện li càng dễ xảy ra, do nhiệt cung cấp năng lượng giúp phá vỡ các liên kết giữa các ion.
- pH của môi trường: Môi trường axit hoặc kiềm có thể ảnh hưởng đến sự cân bằng ion trong dung dịch.
Các Sản Phẩm và Kết Quả của Quá Trình Điện Li
Khi Al₂(SO₄)₃ được hòa tan trong nước, nó phân li thành các ion Al³⁺ và SO₄²⁻. Các ion này có thể tiếp tục tham gia vào các phản ứng hóa học khác, như phản ứng tạo kết tủa hoặc trung hòa axit-bazơ. Ví dụ:
- Ion Al³⁺ có thể phản ứng với OH⁻ trong môi trường kiềm để tạo ra kết tủa Al(OH)₃:
Al3++3OH–→Al(OH)3↓
- Sự thay đổi pH: Quá trình điện li Al₂(SO₄)₃ có thể ảnh hưởng đến độ pH của dung dịch, tùy thuộc vào các phản ứng xảy ra tiếp theo.
Ứng Dụng và Ý Nghĩa Thực Tiễn
Nhôm sunfat (Al₂(SO₄)₃) được sử dụng rộng rãi trong nhiều ngành công nghiệp nhờ vào các tính chất hóa học đặc trưng của nó.
- Trong công nghiệp xử lý nước: Al₂(SO₄)₃ được dùng làm chất keo tụ, giúp loại bỏ các hạt lơ lửng trong nước, tạo ra nước sạch cho sinh hoạt và sản xuất.
- Trong ngành nhuộm vải: Nhôm sunfat hoạt động như một chất cố định màu, giúp màu bám chắc và lâu phai trên sợi vải.
- Trong sản xuất giấy: Al₂(SO₄)₃ được sử dụng để điều chỉnh độ pH và cải thiện chất lượng giấy.
Ngoài ra, Al₂(SO₄)₃ còn có vai trò quan trọng trong nhiều phản ứng hóa học khác, đặc biệt trong nghiên cứu và phát triển các sản phẩm mới trong lĩnh vực hóa học.
Đặc Điểm Vật Lý và Hóa Học của Al₂(SO₄)₃
- Cấu trúc hóa học: Al₂(SO₄)₃ có cấu trúc phân tử phức tạp, gồm hai ion nhôm (Al³⁺) và ba ion sunfat (SO₄²⁻). Mỗi ion sunfat liên kết với ion nhôm thông qua liên kết ion.
- Đặc tính vật lý:
- Màu sắc: Al₂(SO₄)₃ thường có màu trắng hoặc không màu.
- Khối lượng phân tử: 342,15 g/mol.
- Điểm nóng chảy: Al₂(SO₄)₃ tan chảy ở nhiệt độ cao, thường trên 770°C.
- Đặc tính hóa học:
- Phản ứng với axit và kiềm: Al₂(SO₄)₃ có thể phản ứng với các bazơ mạnh để tạo ra kết tủa nhôm hydroxit (Al(OH)₃).
- Phản ứng với các chất khác: Nhôm sunfat tham gia nhiều phản ứng hóa học khác, như phản ứng với muối khác để tạo ra kết tủa mới.
Phương Pháp Điều Chế Al₂(SO₄)₃
- Điều chế trong phòng thí nghiệm: Al₂(SO₄)₃ có thể được điều chế bằng cách cho nhôm phản ứng với axit sulfuric:
2Al+3H2SO4→Al2(SO4)3+3H2
- Sản xuất công nghiệp: Trong công nghiệp, Al₂(SO₄)₃ được sản xuất từ quá trình hòa tan bauxite trong axit sulfuric. Quá trình này tạo ra sản phẩm có độ tinh khiết cao, dùng cho các ứng dụng trong xử lý nước và sản xuất giấy.
Các Phản Ứng Hóa Học Liên Quan
Al₂(SO₄)₃ còn tham gia vào nhiều phản ứng hóa học khác, ví dụ như phản ứng tạo muối với axit sulfuric:
Al(OH)3+3H2SO4→Al2(SO4)3+6H2O
Ngoài ra, Al₂(SO₄)₃ có thể phản ứng với các chất khác để tạo ra các sản phẩm có tính chất khác biệt.
Câu Hỏi Thường Gặp và Bài Tập Minh Họa
- Câu hỏi lý thuyết: Điện li là gì? Al₂(SO₄)₃ sẽ tạo ra những ion nào khi điện li trong nước?
- Bài tập tính toán: Tính nồng độ các ion trong dung dịch khi 5 gam Al₂(SO₄)₃ được hòa tan trong 100 ml nước.
- Đáp án và giải thích chi tiết: Cung cấp lời giải cụ thể cho các bài tập trên để người đọc có thể thực hành và hiểu sâu hơn về chủ đề.
Kết Luận
Phương trình điện li của Al₂(SO₄)₃ không chỉ là một phần quan trọng trong các kiến thức cơ bản về hóa học mà còn có nhiều ứng dụng thực tiễn quan trọng trong cuộc sống và công nghiệp. Hoc vn hy vọng việc nắm vững nguyên tắc, quá trình và các sản phẩm của điện li Al₂(SO₄)₃ giúp chúng ta hiểu rõ hơn về hóa học và ứng dụng của nó trong thực tế.
Xem thêm:
[HƯỚNG DẪN] Giải Bài Tập Một Oxit Nito Có Công Thức NOx
[GIẢI ĐÁP] MgCl2 Là Chất Điện Li Mạnh Hay Yếu?